王伟医生的科普号
- 精选 得了胆囊结石怎么办?
胆囊结石分为症状性胆囊结石和无症状性胆囊结石:一. 症状性胆囊结石就是引起患者不适或急性胆囊炎发作的胆囊结石。治疗方案:需要手术,首选腹腔镜胆囊切除术,一般在急性发作后一个月手术。注意:因胆囊结石引起的腹部不适有的时候和胃病相似,如果没有明确的急性胆囊炎发作病史,建议手术前行胃镜检查排除胃病后再做手术,如有胃病先行胃病治疗。二. 无症状性胆囊结石就是患者虽然有胆囊结石,但并没有引起患者不适或急性胆囊炎发作。对于这一类患者有以下情况需要手术,首选腹腔镜胆囊切除术:1.结石大小超过3cm。2.伴有胆囊息肉。3.伴有胆囊壁增厚或钙化。4.伴有胆囊萎缩。5.伴有糖尿病。6.生活在边远地区,发作胆囊炎来不及治疗。如果没有上述情况,可定期复查B超,一般半年至一年复查一次。
王伟 副主任医师 上海市第六人民医院 肝胆胰外科3997人已读 - 精选 得了胆囊息肉怎么办?
1. 胆囊息肉样病变≥10 mm,推荐胆囊切除术。2. 胆囊息肉病人症状与胆囊相关,找不到其他原因,建议行胆囊切除术。3. 如不符合上述两项条件,应评估病人胆囊恶性肿瘤的危险因素:年龄>50岁;原发性硬化性胆管炎(PSC)病史;印第安族群;无蒂息肉(包括局限性胆囊壁增厚,厚度>4 mm)。3.1 如果病人存在胆囊恶性肿瘤风险因素且息肉大小6~9 mm,推荐胆囊切除术。3.2 如果病人存在胆囊恶性肿瘤风险因素且胆囊息肉≤5 mm,建议在6个月、1年,然后每年直至5年做随访超声检查。3.3 如果病人没有胆囊恶变危险因素且胆囊息肉6~9 mm;建议在6个月、1年,然后每年直至5年做随访超声检查。3.4 如果病人没有胆囊恶变危险因素且胆囊息肉≤5 mm,建议在第1年、3年和5年做随访。6. 随访期间胆囊息肉增加≥2 mm,建议行胆囊切除术。7. 随访期间胆囊息肉达到10 mm,建议胆囊切除术。8. 随访期间胆囊息肉消失则停止随访。9.基本检查是用腹部超声。不建议常规使用其他影像学检查。
王伟 副主任医师 上海市第六人民医院 肝胆胰外科3466人已读 - 精选 肝内胆管结石的诊治
肝胆管结石病即原发性肝胆管结石特指始发于肝内胆管系统的结石。由于其病变复杂、复发率高且常引起严重的并发症,此病成为我国良性胆道疾病死亡的重要原因。1. 肝胆管结石病的病因和基本病理改变(1)肝胆管结石病的病因目前还不完全清楚。肝内结石的形成与胆道慢性炎症、细菌感染、胆道蛔虫、胆汁淤滞、营养不良等因素有关。(2)胆汁流动缓慢并有胆道慢性炎症最易形成肝内胆管结石。肝胆管结石病的基本病理改变是胆道梗阻、胆道感染和肝实质破坏。2.肝胆管结石常见并发症(1)重症急性胆管炎(2)胆源性肝脓肿(3)胆道出血(4)肝胆管癌 约2.0%~9.0%在病程后期可并发肝胆管癌。(5)胆汁性肝硬化及门静脉高压症3. 肝胆管结石病的临床表现可分为3大类型:(1)静止型:患者无明显症状或症状轻微,仅有上腹隐痛不适,常在体检时才被发现。(2)梗阻型:表现为皮肤眼睛发黄、右中上腹持续性疼痛不适、消化功能减退等胆道梗阻症状。(3)胆管炎型:表现为反复发作的急性化脓性胆管炎。4. 肝胆管结石病的诊断有实用价值的影像技术主要有B超、CT、磁共振。单一的检查常不能获得全面的诊断,往往需要一种以上的影像学检查相互印证才能达到正确诊断的目的。5. 肝胆管结石病的治疗(1)有明显临床症状的患者需要治疗。(2)对于症状不明显的静止型结石是否需要治疗,目前的意见尚未统一。鉴于随病程演进和病变发展,多数病例将出现明显症状且有受累肝管恶变的可能,对于静止型结石也多主张积极治疗。(3)治疗主要靠外科手术,包括:胆管切开取石术;肝部分切除术;肝门部胆管狭窄修复重建术;肝移植术。
王伟 副主任医师 上海市第六人民医院 肝胆胰外科2595人已读 - 学术前沿 超微创:单孔腹腔镜胆囊切除
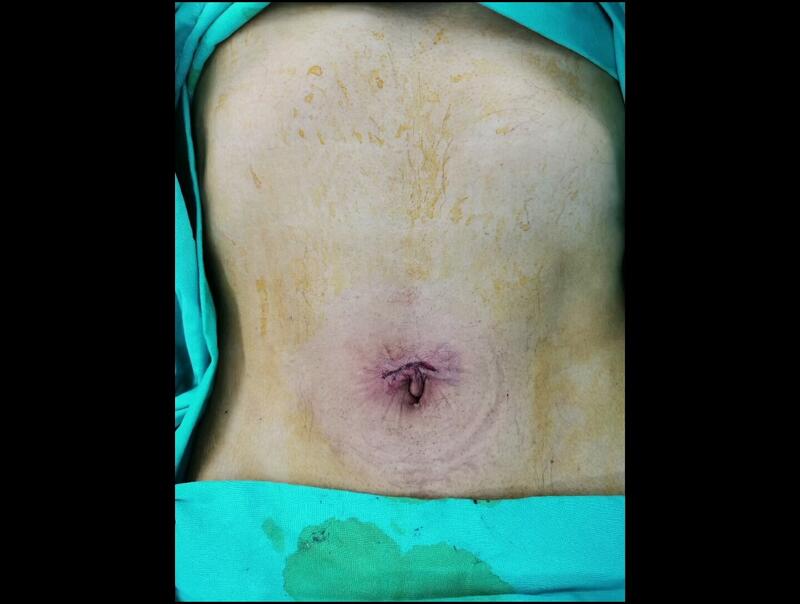 王伟 副主任医师 上海市第六人民医院 肝胆胰外科97人已观看
王伟 副主任医师 上海市第六人民医院 肝胆胰外科97人已观看 - 论文精选 胰门板降低技术在胰腺段胆总管囊肿切除术中的应用价值
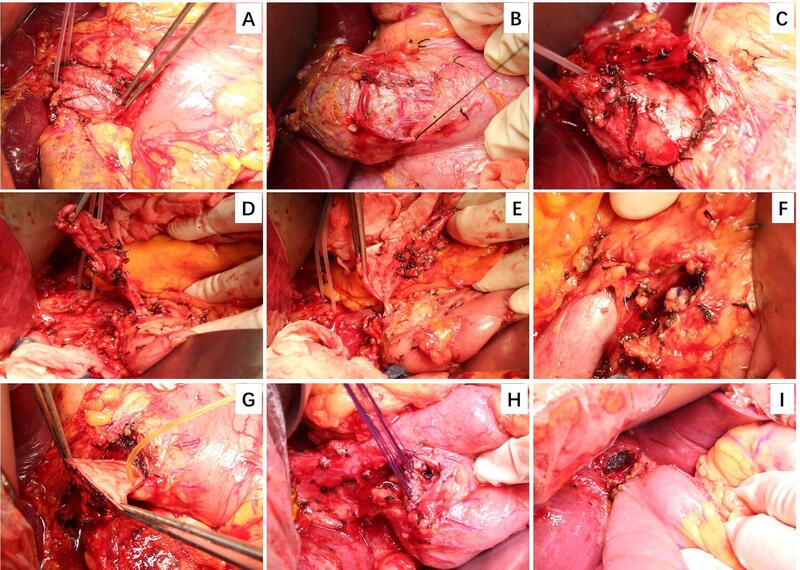
胆总管囊肿的手术原则是彻底去除病变胆管组织,实现胆胰分流,达到解决胆汁淤滞、胆道感染和防止癌变的目的,因此囊肿彻底切除联合肝管空肠吻合术是较为公认的治疗胆总管囊肿的手术方式。对于胰腺段胆总管囊肿,常规采用挖地雷似地剜除式切除术,但该手术在实际操作中很难彻底切除囊肿且风险较大,因此有不少学者采用该方法行囊肿部分或大部切除术时,易出现部分胰腺段囊性扩张胆管残留,从而使残留囊壁癌变,并引起残留囊性扩张胆管内胰液潴留,进而导致蛋白栓、结石及术后急性胰腺炎等并发症发生。因此,安全彻底地切除包括胰腺段在内的囊性扩张胆管且不损伤主胰管,对于防止残留胰腺段囊肿癌变、减少术后胰腺并发症等十分必要。 了解胰腺段囊性扩张胆管的解剖层次和血供特点,对指导手术切除至关重要。相关文献报道,胰腺内囊性扩张胆管由内向外由黏膜层、固有层及纤维结缔组织层组成,其血供主要来自胰十二指肠上的动脉分支;这些血管分支可形成血管丛,分布于囊性扩张胆管的纤维结缔组织层表面,包绕囊性扩张胆管并向壁内深入,形成两个壁内血管丛,分布于纤维结缔组织层与固有层之间以及固有层与黏膜层之间。因此,我们在行胰腺段囊性扩张胆管切除时可结扎胃十二指肠动脉,阻断胰腺段囊肿血供,从而减少分离过程中的出血。在胰腺段囊性扩张胆管的纤维结缔组织层与前方的胰腺实质之间,如同肝门板与前方肝实质一样,存在天然的解剖间隙,其可为显露胰腺段胆管提供了天然的解剖路径。基于此,本课题组将胰腺段囊性扩张胆管的纤维结缔组织层视为胰门板,运用胰门板降低技术(如同降低肝门板一样),沿胰腺段胆管与胰腺组织之间进行分离,仔细结扎切断囊肿和胰腺之间的小血管,逐步下翻胰腺来实现胰腺段胆管囊肿的游离直至胆胰管汇合处。该方法不仅可以全程显露胰腺段胆管,控制术中出血,还有助于识别狭小的胆管末端和胆胰管汇合方式,以增加手术的安全性(图1)。 图1 采用胰门板降低技术行胆总管囊肿切除手术过程 胰腺段胆总管囊肿切除术中还应注意主胰管大致走行方向、胆管下段狭窄段的长度,特别是胆胰管汇合方式,以避免主胰管损伤、术后难治性胰漏和急性胰腺炎的发作。根据本研究纳入的胰腺段胆总管囊肿患者情况,我们将其胆胰管汇合方式分为2 类,一类是主胰管与胆总管囊肿远端的正常胆管汇合,另一类是主胰管与胆总管囊肿汇合(图2)。研究显示,术前CT、MRCP、内镜下逆行胰胆管造影术和皮肝穿刺胆道造影术检查有助于观察胆胰管全貌,对指导处理胆胰管连接部和避免主胰管损伤有重要的参考价值;且在以往的临床实践中,临床医师主要根据术前影像资料或术中胆胰管造影所示的胆胰管连接部形态,结合囊内插入探针引导或胆道镜引导等方法识别、确认胆管末端及主胰管开口。而通过上述方法确认胆胰管的汇合方式是间接的,或相对盲目。本研究采用的胰门板降低技术可全程显露胰腺段胆管直至胆胰管汇合处,能够在直视下探查胆胰管的汇合方式,有利于完整切除胆胰管连接部以上胆管,并最大限度地避免主胰管损伤;同时,在充分显露胆胰管汇合处的情况下,即使发生主胰管损伤,也可及时发现并加以修复,以避免胰漏的发生。 图1 胰腺段胆总管囊肿与主胰管的汇合方式示意图 在胆管囊肿完整切除后,临床医师应常规仔细检查胆管壁情况,如见异常隆起、胆管腔内见黏冻样物质而疑似癌变时,应及时行术中冰冻病理检查;如为癌变,需即刻施行胰十二指肠切除术,以实现对胰腺段胆管囊肿癌变的根治。对于囊肿切除后的胰腺创面,可在术中予以间断缝合关闭,以避免创面渗血、消除肉眼未能发现的细小胰漏,并于术后酌情使用生长抑素类药物来减少胰漏;但当创面过大或过深导致缝合困难时,则可予大网膜填塞,同时勿过早拔除引流管,持续敞开冲洗引流,从而减少胰漏的发生。 综上所述,胰门板降低技术可以全程显露胰腺段胆总管直至胆胰管汇合处,是安全彻底切除胰腺段囊性扩张胆管的重要保障。该技术在治疗胰腺段胆总管囊肿的实际应用过程中安全可行,疗效满意,或将成为切除胰腺段胆总管囊肿的一种新方法。
 王伟 副主任医师 上海市第六人民医院 肝胆胰外科336人已读
王伟 副主任医师 上海市第六人民医院 肝胆胰外科336人已读 - 精选 胰门板降低技术取出嵌顿于胰腺段胆总管的巨大结石
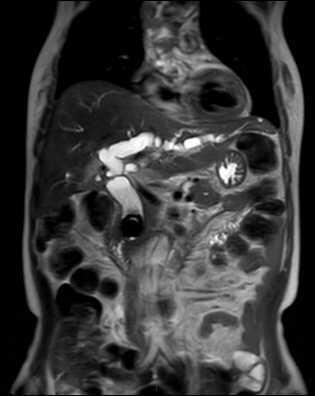
胆总管末端结石嵌顿属于复杂肝外胆管结石的治疗范畴,是肝外胆管结石处理的难点,处理不当会导致胆胰肠结合部损伤、急性胰腺炎、胆道出血和结石残留等并发症。对于质硬的胰腺段胆总管巨大结石嵌顿的治疗难点在于既难以通过Oddi括约肌切开,经十二指肠乳头取出,也难以通过胆总管前壁切开,经胆总管取出。若结石质硬无法通过碎石后取出,此时主要的手术难度是缺乏可供取石器械操作的空间,取石钳和取石网篮往往难以越过结石,无法行有效的抓取和套取,相当于嵌顿疝不打开狭窄环无法取出结石,而此狭窄环位于胰腺段胆总管,只有打开狭窄环才能取出嵌顿结石。既往有学者取Kocher切口,游离十二指肠和胰头向左翻起,采取“上取下推”的手法,即一边从下往上推结石、一边从胆总管开口取结石的方法,取出胰腺段胆总管嵌顿结石[3]。还有学者将十二指肠后段胆总管的前壁切开后取出胰腺段胆总管嵌顿结石。但这些方法无法打开位于胰腺段胆总管的狭窄环,在面临胰腺段胆总管较大结石嵌顿的情况时,还是难以取出结石。 本团队创立的“胰门板降低技术”从上而下全程切开胰腺段胆总管,才能取出结石。与肝脏包绕胆管、肝动脉和门静脉形成肝门结构类似,胰腺也包绕进入胰腺实质的胆总管胰腺段,笔者将此结构称为“胰门”,敞开胰门来显露胆总管胰腺段的操作称为“胰门板降低技术”。采用此技术如同降低肝门板一样,沿胰腺段胆管与胰腺组织之间分离,下翻十二指肠球部和胰头组织,进一步向下显露胰腺段胆总管的前壁直至狭窄环,切开此狭窄环后就能顺利取出嵌顿的铸形结石。胰腺段胆总管与胰腺组织之间存在天然的解剖间隙,其间并无重要结构,遇到小的血管可仔细结扎切断,技术可行。总之,鉴于胆总管胰腺段解剖的特殊性,在行此段胆总管嵌顿结石取出时应掌握正确的技巧,降低胰门板技术可充分显露胰腺段胆总管前壁,为取出结石提供了有效的解剖路径,可以最大限度地避免胆胰肠结合部的医源性损伤。 案例: 患者女性,64岁,因“皮肤巩膜黄染伴恶心呕吐半年余”入院,无发热、腹痛、腹胀等。 查体:生命体征平稳,皮肤巩膜黄染。全腹软,无明显压痛,无反跳痛、肌紧张,墨菲征阴性。 实验室检查:血常规:WBC 7×109/L,中性粒细胞 66.2%;肝功能:ALT 48 U/L,AST 46 U/L,TBIL 54.6 μmol/L,DBIL 41.4 μmol/L,AKP 623 U/L,γ-GT 631 U/L;乙肝表面抗原阴性。 影像学检查:腹部彩超示肝内胆管扩张,胆囊显示不清,胆总管扩张,胆总管内条状等回声物;上腹部平扫MRI/MRCP示胆总管下段结石伴肝内外胆管扩张,胆囊未见,肝门区多发增大淋巴结。 术前诊断为:(1)胆总管结石;(2)胆囊萎缩。 拟行腹腔镜下胆囊切除术+胆总管切开取石+T管外引流术。 但是术中发现横结肠和十二指肠与肝脏面和第一肝门致密黏连,胆囊萎缩,大小约5 cm ×3 cm ×2 cm,与横结肠形成内瘘,胆囊三角区呈胼胝样。胆总管扩张,直径约2 cm,充满墨绿色胆汁,胰腺段胆总管内含一枚直径约2.5 cm混合性结石。术中诊断:(1)胆总管结石,(2)胆囊结肠瘘。 遂行腹腔镜中转开腹胆囊切除+胆总管切开取石+胆道镜探查+T管外引流+结肠瘘修补+肠黏连松解术。术中运用胰门板降低技术顺利取出胰腺段胆总管内含嵌顿的一枚直径约2.5 cm结石。 术后6周T管造影未见结石残留和胆管狭窄后拔除T管。术后门诊随访至今,患者一般情况良好,复查肝功能和腹部B超未发现结石复发和胆管狭窄。
 王伟 副主任医师 上海市第六人民医院 肝胆胰外科341人已读
王伟 副主任医师 上海市第六人民医院 肝胆胰外科341人已读 - 医学科普 胆管扩张症的诊断与治疗
胆管扩张症,又称胆管囊肿,是临床较少见的一种原发性胆管病变,可由婴幼儿时期先天性胆管扩张延续而来,也可在成年期发病,主要表现为肝内、外胆管单发或多发性局部扩张。女性发病率为男性的3~4倍,多发病于婴幼儿时期和儿童期,约20%发病于成年期。1病因病因复杂,目前主要有遗传学因素、胰胆管合流异常、胃肠道神经内分泌、胆管上皮异常增殖、其他因素(如病毒感染、妊娠、胆管炎症等)。2临床表现腹痛、腹上区包块和黄疸为BD的三大主要临床表现,但三者同时出现较为少见(发生率为20%~30%)。不同年龄段的患者临床表现差异明显。婴幼儿及儿童患者主要临床表现为明显的腹部包块和梗阻性黄疸,成人患者则主要表现为腹痛。3并发症胆管扩张症患者并发症发生率为20.0%~60.0%,常见并发症包括胆道结石、胰腺炎和胆道癌变;其他并发症有复发性胆管炎、门静脉高压症、自发性囊肿破裂等。这是对该病应及时治疗的依据,尤其是可并发胆道癌变。4诊断方法彩色多普勒超声检查是主要筛查手段。多排螺旋CT检查在评估病变胆管周围解剖关系和是否存在并发症上具有优势。MRCP检查可作为诊断的首选方法。ERCP、PTC、术中胆道造影、术中胆道镜检查可作为补充诊断或治疗手段,有助于更加精确、全面地评估病变情况。目前尚无针对胆管扩张症的特异性血液学诊断指标。5治疗国内外学者一致认为:不论是否有临床症状,一旦确诊胆管扩张症,应尽早行手术治疗,降低胆道癌变率;暂时不能行手术治疗者,建议每6个月定期随访观察。6随访建议手术患者术后半年内每3个月、半年后每6个月复查血常规、肝功能、血清淀粉酶、肿瘤标志物(CA19-9、CEA等)及腹部彩色多普勒超声、CT、MRI等影像学检查。
王伟 副主任医师 上海市第六人民医院 肝胆胰外科6063人已读 - 论文精选 黄色肉芽肿性胆囊炎诊治分析
黄色肉芽肿性胆囊炎(xanthogranulomatous cholecystitis,XGC)于1970年由Christensen和Ishak首先报道。目前认为,XGC是由长期反复发作的胆囊慢性炎症缓慢进展而来,其确切的发病机制还不明确。XGC的临床表现与急性或慢性胆囊炎相似。当胆囊壁肉芽肿压迫胆总管时还可有阻塞性黄疸的表现,类似于Mirizzi综合征的症状。肿块巨大时在右上腹可触及包块。本组资料中,20例表现为右上腹痛,占76.9%;其中12例表现为急性胆囊炎症状,4例表现为慢性胆囊炎症状,4例表现为右上腹痛伴有黄疸的Mirizzi综合征;其余6例无症状,可见XGC的临床表现主要以胆囊炎症状为主。XGC的术前诊断一直是临床一大难点,B超对于合并有胆囊壁明显增厚或肝脏浸润的XGC诊断准确率不高。本组资料中,术前B超明确诊断出胆囊炎者只占61.5%。影像学检查的联合应用是否可提高XGC的诊断率还有待探讨。本组资料中,B超联合CT+MRI+PET—CT检查1例,虽倾向于炎症,但仍无法排除胆囊癌。B超联合CT+MRI检查4例中,2例排除胆囊癌。B超联合CT检查2例,未能排除胆囊癌。影像学联合检查的术前诊断准确率由单用B超检查的61.5%提高到69.2%,虽然有一定的提高,但还是无法完全明确诊断。目前,病理检查仍是诊断XGC的金标准,特别是术中快速病理检查对于术中排除胆囊癌十分重要。有时需多处、多点取材,包括周边包裹组织做快速冰冻病理检查,以避免误诊为胆囊癌而行扩大手术给患者带来不必要的创伤。本组资料中有8例患者术前无法排除胆囊癌,术中行病理检查,最终均确诊为XGC。因此,术中快速病理检查应作为常规,切下完整标本应再送冰冻病理检查,再次排除胆囊癌。XGC最典型的病理特征为镜下泡沫细胞,有时整个胆囊壁可见炎症细胞浸润。XGC长期慢性进展是否会转变为胆囊癌目前还无定论。有文献报道XGC存在癌变的可能性,胆囊腺癌中有10%存在XGC,XGC标本中也有10%发现腺癌。因此,对于确诊为XGC的患者主张早期手术,手术主要为胆囊切除。本组资料中行单纯胆囊切除术者20例,其中16例尝试行腹腔镜胆囊切除术,但中转开腹10例,占62.5%。XGC常伴有腹腔粘连及胆囊三角解剖不清,导致腹腔镜下手术存在一定困难,易导致胆管损伤,需慎重选择。笔者认为,能否行腹腔镜手术取决于术前能否明确诊断。若无法排除胆囊癌,又与周边组织包裹,考虑手术难度及烟囱效应不应行腔镜手术。若术前排除胆囊癌且炎症不严重,则可考虑行腹腔镜胆囊切除术。对于急性胆囊炎发作又伴有腹腔严重粘连、患者一般条件差者,在冰冻病理排除胆囊癌后还可选择胆囊大部切除术,尽量缩短手术时间,提高手术安全性。对于病变浸润至肝脏及胆囊周围其他组织者,是否需行受侵脏器联合切除目前还存在争论。本组中就有2例XGC患者因存在肝脏浸润行胆囊切除+肝楔形切除。其原因在于切下标本前无法确诊是否为胆囊癌,为达到整块切除的目的行胆囊切除+肝楔形切除术。这2例患者最终术中冰冻病理均提示胆囊炎症。笔者认为,对于合并肝脏浸润的XGC,若术中无法排除胆囊癌,为达到整块切除效果,可选择行胆囊切除+肝楔形切除术。对于合并Mirizzi综合征的XGC患者,可行胆总管切开整形T管外引流术。本组资料中有4例患者因与胆总管形成内瘘而行胆囊切除+胆总管整形T管外引流。术前对XGC与胆囊癌做出一个正确的鉴别诊断仍是目前临床的一大难题,特别是那些伴有周围组织或器官侵犯的病例。术中冰冻病理检查则是XGC确诊的金标准。对于伴有周围组织浸润的XGC患者,是否行胆囊+周围受侵组织切除术目前还没有定论,手术方式仍以胆囊切除术为主。腹腔镜胆囊切除术的选择需慎重,切勿为追求微创而导致胆管及邻近脏器的损伤。对于合并肝脏浸润的病例,可行肝楔形切除术。在冰冻病理未做之前不宜盲目行肝段与肝叶切除。
王伟 副主任医师 上海市第六人民医院 肝胆胰外科2806人已读 - 论文精选 胆总管神经内分泌肿瘤的诊断和治疗
神经内分泌肿瘤起源于Kulchitsky细胞,此种细胞可见于消化系统和呼吸系统的多个部位,而在胆道中数量极少,因此,肝外胆管发生神经内分泌肿瘤极其罕见,据报道其发生率在整个消化系统占0.32%[1],在所有患者占0.2-2%[2]。在肝外胆管中,最常见的部位是肝总管和胆总管末段(19.2%),其次是胆总管中段(17.9%)、胆囊管(11.5%)和胆总管近段(11.5%)[2]。根据生长情况,肝外胆管神经内分泌肿瘤大体分为三个类型:结节型、胆管内生长型和周围浸润型。本例患者肿瘤位于胆总管末段,为结节型,其特点为向腔内凸起生长的结节,而表面粘膜光滑。由于肝外胆管神经内分泌肿瘤罕见,所以其临床病理特征尚不明了,导致其术前难以确诊。据以往文献报道,其好发于女性,男女比例为1:1.6,好发年龄为50-60岁[2]。胆管神经内分泌肿瘤早期缺乏特异的临床症状,以梗阻性黄疸为首发症状的最常见,其他依次为腹痛、瘙痒、恶心呕吐以及体重减轻等,部分患者可合并胆石症。而典型的类癌综合症少见,包括痉挛性腹痛、面色潮红、腹泻、水肿、哮喘、心脏病、糙皮病等。本例患者因肿瘤位于胆管末端致胆道梗阻,故以急性胆道感染和梗阻性黄疸发作为首发症状。因同时合并有胆囊小结石,致临床症状上有更大的迷惑性,容易被误诊为继发性胆总管结石。影像学检查有助于肿瘤的定位和定性。B超检查缺乏特异性表现,只能作为初步筛查。CT可显示肿瘤的部位,在动脉期强化程度往往高于或等于肝实质,在静脉期强化程度往往等于或低于肝实质,并且有助于判断血管侵犯和淋巴结转移。而本例患者在动脉期强化程度等于肝实质,在静脉期强化程度高于肝实质,给术前影像学诊断带来困难。MRI、MRCP有助于判断肿瘤类型,在T1加权像肿瘤密度低于肝实质,T2加权像肿瘤密度高于肝实质,DWI成像肿瘤密度高于肝实质,动脉期肿瘤密度往往低于或等于肝实质,静脉期肿瘤密度往往低于肝实质。ERCP不仅可以发现肿瘤,还可以取活检,但是胆管神经内分泌肿瘤位于黏膜下,假阴性率较高。本例患者MRI和ERCP并没有发现肿瘤,可能与肿瘤较小且位于粘膜下有关。PET-CT有助于判断肿瘤的良恶性,神经内分泌癌的中位SUV为8.1[3]。病理学检查不仅是确诊本病的主要手段,而且是肿瘤分级的主要依据。免疫组化染色CgA和突触素(Synaptophysin,SYN) 阳性可确诊。其他可选择的检查项目包括CD56、激素、生长抑素受体2亚型、淋巴血管标记物和P53等。本例病人CgA和SYN均染色阳性,确诊为胆管神经内分泌瘤。2010版WHO神经内分泌肿瘤分级着重强调肿瘤细胞分化程度:G1,核分裂象数<2和/或Ki-67指数<2 %;G2,核分裂象数2–20和/或Ki-67指数3-20%;G3, 核分裂象数>20和/或Ki-67指数>20%。G1、G2为神经内分泌瘤,G3为神经内分泌癌。本例患者Ki67<1%,为G1期神经内分泌瘤。手术是治愈的唯一手段。一旦发现胆管的神经内分泌肿瘤,尽早行根治性手术切除,5年生存率达到67%,即使出现转移,2年生存率也达到60%[4]。手术范围包括病变胆管切除联合淋巴结清扫。胆总管下段肿瘤选用胰十二指肠切除手术;胆总管上段和中段肿瘤应整块切除肝外胆管上至肝总管、下至胰腺上缘,包括周围淋巴组织;肝门胆管肿瘤应联合肝切除,以达到根治的目的。即使有肝转移,也应考虑手术治疗,应尽力切除原发灶及转移灶。也有少数病例报道可行局部切除,但疗效有待进一步证实。因此,本例患者肿瘤位于胆总管末端,在术中冰冻病理无法明确肿瘤性质的情况下,放弃局部切除,改行胰十二指肠切除术较为稳妥。胆管神经内分泌肿瘤根治性切除术后的辅助治疗目前尚无高级别的循征医学证据。参照同为前肠来源的胰腺发生神经内分泌肿瘤时所采用的辅助治疗原则,不推荐对根治术后的G1/G2患者进行辅助性药物治疗。对于根治术后的G3患者,医师可根据手术情况决定是否行辅助全身治疗和(或)局部放射治疗[5]。目前可用的辅助性治疗手段包括:全身化疗(根据NCCN指南,参照小细胞肺癌化疗方案)[6]、靶向治疗、生长抑素以及放疗等。本例患者术后病理证实G1期神经内分泌肿瘤,故术后未予放化疗。总之,胆总管神经内分泌肿瘤是少见疾病,术前难以确诊,完善有序的检查,仔细观察影像学检查中的细节,充分的术前评估,制定合理的手术方案,可避免误诊的发生。目前根治性手术切除是治愈的唯一手段。
王伟 副主任医师 上海市第六人民医院 肝胆胰外科3823人已读






